Au cours du développement du cerveau, les milliards de cellules composant le système nerveux établissent entre elles des connexions spécifiques afin de former un réseau fonctionnel. L’établissement de ces circuits repose sur un processus appelé « guidage axonal », au cours duquel les axones voyagent sur des distances plus ou moins longues et se connectent à leurs neurones cibles. Chez la plupart des animaux, ces processus sont plus complexes au niveau du cerveau qu’au niveau de la moelle épinière. Des défauts dans la formation des connexions cérébrales pendant le développement embryonnaire peuvent conduire à différents types de pathologies neuronales. Ainsi, la compréhension de la formation des connexions cérébrales pendant le développement normal du cerveau pourrait aider à traiter certaines maladies ou lésions cérébrales.
Grâce à l’étude de la formation des connexions cérébrales chez la drosophile via une voie de signalisation très conservée, l’équipe de Bassem Hassan, Directeur de recherche Inserm et chef d’équipe à l’Institut du Cerveau – ICM, a mis en évidence que le guidage axonal dans le cerveau permet beaucoup plus de flexibilité et d’auto-organisation car une population particulière de neurones guide d’autres populations de neurones. Ils ont également décrit le mécanisme moléculaire de la formation de ces connexions via une protéine nommée RPTP69d. Ces résultats ont été publiés dans la revue Developmental Cell, le 24 Octobre 2016.
Au cours du développement du système nerveux, les neurones établissent entre eux de nombreuses connexions pour former un réseau fonctionnel. L’établissement de ces circuits repose sur un processus appelé « guidage axonal », au cours duquel les axones voyagent sur des distances plus ou moins longues et se connectent à leurs neurones cibles. Le développement du système nerveux implique un processus nommé guidage axonal, qui est le processus d’amener les nerfs à la bonne place dans le cerveau. C’est l’interaction de récepteurs présents à la surface des neurones avec des molécules attractrices ou répulsives présentes dans leur environnement qui permet la mise en place de ce processus.
L’équipe de Bassem Hassan a étudié la formation des connexions cérébrales au cours du développement chez la drosophile. La formation de ces connexions est en effet beaucoup plus complexe au niveau du cerveau qu’au niveau de la moelle épinière.
Dans la moelle épinière de drosophile (appelée corde nerveuse ventrale), une ligne de cellules non neuronales (cellules gliales) au milieu de la structure (ligne médiane) agit comme source de molécules de guidage, attractrices ou répulsives. Les axones possèdent des récepteurs pour ces molécules et en fonction du type de récepteur, les axones vont s’approcher ou non de cette ligne, être attirés ou repoussés et ne la traverseront éventuellement qu’une seule fois. Dans la moelle épinière, les cellules gliales sécrètent une protéine nommée Slit pour guider les axones exprimant le récepteur de Slit nommé Robo.
Dans le cerveau, la formation des connexions est beaucoup plus complexe car cette source médiane de molécules de guidage n’existe pas.
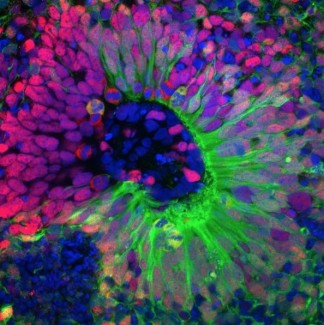
Des chercheurs de l’équipe de Bassem Hassan ont mis en évidence que la protéine Slit est exprimée par les « neurones de la mémoire » dans le cerveau de la drosophile (appelés les Mushroom bodies), qui envoient leurs extensions (axones et dendrites) au sein de nombreuses parties du cerveau. La molécule Slit est ainsi distribuée vers différentes populations neuronales à partir d’une seule population de neurones. L’expression de Slit au niveau de ces dendrites et axones va permettre le guidage d’autres axones exprimant le récepteur Robo.
Les chercheurs ont également montré que les neurones exprimant Slit n’expriment pas de récepteurs Robo. Ce mécanisme permet à un neurone de communiquer à un autre neurone comment et jusqu’où croître. Les neurones ne possédant pas de récepteurs Robo ne réagissent pas à Slit. En d’autres termes, les neurones du cerveau auto-organisent leurs propres circuits.
Une réorganisation du cerveau serait donc possible en modifiant les quantités respectives des différentes populations de neurones. La modification de l’expression des molécules Slit et Robo pourraient modifier la formation des connexions cérébrales, créant ainsi une plus grande flexibilité. De manière intéressante, chez la mouche, une seule population de neurones exprime Slit, mais il est envisageable que dans des cerveaux plus complexes, différentes populations neuronales expriment cette molécule, entraînant ainsi une sorte de jeu entre les cellules qui s’éviteraient les unes les autres.
Comment sont régulés les récepteurs Robo, indispensables au guidage axonal, à la surface des neurones ? Les chercheurs ont mis en évidence que la protéine qui régule Robo dans le cerveau n’est pas la même que dans la moelle épinière.
Un candidat potentiel est une famille de protéines transmembranaires, les récepteurs de phosphatases. Ces récepteurs de phosphatases sont présents sur la membrane des axones. Leur partie intracellulaire agit comme une enzyme en modifiant chimiquement d’autres protéines. Les chercheurs ont montré qu’un de ces récepteurs, RPTP69d, régule la quantité de Robo au niveau de la membrane. Plus il y a de RPTP69d, plus il y a de récepteurs Robo présents sur la membrane. En l’absence de RPTP69d, cependant, les axones se comportent comme s’ils ne possédaient pas la molécule Robo.
Le rôle de RPTP69d dans l’expression de Robo à la surface des cellules est indépendante de son activité enzymatique, cette protéine forme un complexe avec Robo et le stabilise à la surface des cellules.
Ce travail met en évidence une fonction jusqu’alors inconnue des « neurones mémoires » de la drosophile, les mushroom bodies, dans la formation des connexions cérébrales et l’implication des récepteurs Robo et de leurs ligands Slit dans ce mécanisme.
Ces récepteurs jouent également un rôle important dans la formation des connexions cérébrales chez l’Homme et la protéine Robo3 est mutée chez les patients atteints de horizontal gaze palsy with progressive scoliosis (HGGPS), une maladie neurologique rendant impossible le mouvement horizontal des yeux et causant une courbure anormale de la colonne vertébrale (scoliose). De plus, les récepteurs Robo jouent un rôle dans la formation des vaisseaux sanguins. Slit et Robo sont également tous deux impliqués dans de nombreux de types de cancers chez l’homme.
La compréhension de la façon dont Robo est régulé pourrait donc ouvrir des perspectives thérapeutiques pour certaines maladies neuronales mais également pour certains types de cancers.
Slit, Robo et RPTP69d étant des protéines très conservées entre les espèces, les chercheurs envisagent d’étudier ce nouveau mécanisme moléculaire plus largement, dans les systèmes mammifères.
Sources
https://pubmed.ncbi.nlm.nih.gov/27780041/
Carlos Oliva, Alessia Soldano, Natalia Mora, Natalie De Geest, Annelies Claeys, Maria-Luise Erfurth, Jimenna Sierralta, Ariane Ramaekers, Dan Dascenco, Radoslaw K. Ejsmont, Dietmar Schmucker, Natalia Sanchez-Soriano and Bassem A. Hassan.