Porteur de projet, MD, PhD, MCU-PH, Responsable d'équipe, PI, Sorbonne Université, AP-HP

Porteur de projet, MD, PhD, MCU-PH, Responsable d'équipe, PI, Sorbonne Université, AP-HP
Présentation de l'équipe
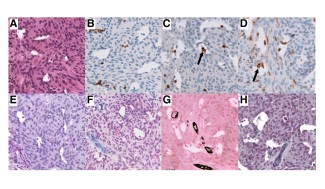
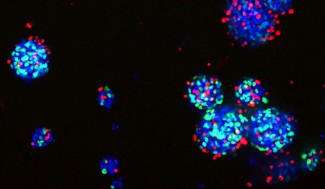
Le laboratoire vise à comprendre les altérations génétiques et du microenvironnement tumoral au cours de l’évolution des tumeurs cérébrales, et à déterminer comment ces altérations influencent le comportement des tumeurs et leur réponse aux traitements, avec pour objectif d’améliorer les stratégies thérapeutiques. Dans ce but le laboratoire utilise des échantillons de patients issus de la chirurgie et de nombreux modèles précliniques in vitro et in vivo.
Nos travaux de recherche s’articulent autour de trois axes principaux
- Améliorer la compréhension de l’hétérogénéité tumorale afin de mieux prédire le pronostic des patients et leur réponse aux traitements
- Identifier et cibler les mécanismes sous-jacents à la résistance aux traitements dans les tumeurs cérébrales
- Moduler les interactions entre les cellules tumorales et du microenvironnement afin d’optimiser de nouveaux traitements notamment d’immunothérapie
Quelques projets phares de l’équipe
- Étude intégrée de l’hétérogénéité des tumeurs cérébrales (glioblastomes, gliomes IDH-mutés, lymphomes cérébraux et tumeurs rares), combinant analyses multi-omiques (génétiques épigénétiques, transcriptomiques, histomiques), exploration des interactions avec le microenvironnement tumoral, et développement d’outils innovants en imagerie avancée et en intelligence artificielle (Porteurs : Agusti Alentorn, Franck Bielle, Francesca Branzoli, Khê Hoang-Xuan)
- Caractérisation des mécanismes de résistance aux chimiothérapies et aux immunothérapies et développement de nouvelles stratégies thérapeutiques, notamment dans le glioblastome, visant à améliorer le pronostic des patients, par l’utilisation de modèles de type lignées dérivées de patient, xénogreffes, tumoroïdes et organoïdes (Porteurs : Ahmed Idbaih, Isabelle Le Roux, Mehdi Touat, Maïté Verreault)
- Étude des interactions entre les cellules tumorales et leur microenvironnement, en particulier les cellules myéloïdes et lymphoïdes et le réseau vasculaire, afin d’identifier des biomarqueurs prédictifs de réponse et de caractériser les synergies thérapeutiques (Porteurs : Luis J. Castro-Vega, Ahmed Idbaih, Isabelle Le Roux, Michel Mallat, Marc Sanson, Mehdi Touat)
2025
- Kacimi S et al. Survival Outcomes Associated With First-Line Procarbazine, CCNU, and Vincristine or Temozolomide in Combination With Radiotherapy in IDH-Mutant 1p/19q-Codeleted Grade 3 Oligodendroglioma. J Clin Oncol . 2025 Jan 20;43(3):329-338.
- Nichelli L et al. Incorporation of Edited MRS into Clinical Practice May Improve Care of Patients with IDH-Mutant Glioma. AJNR Am J Neuroradiol. 2025 Jan 8;46(1):113-120. doi: 10.3174/ajnr.A8413.
- Hernández-Verdin I et al. Gut microbiome modulates the outcome in primary central nervous system lymphoma patients undergoing chemotherapy: An ancillary study from the BLOCAGE trial. Neuro Oncol. 2025 Sep 17;27(8):2090-2104.
- Morfouace M, Bielle Fet al. Molecular analysis of adolescent and young adult high grade gliomas in the SPECTA-AYA study: Poorly characterised tumours with frequent germline alterations. Eur J Cancer. 2025 Jun 18;223:115493.
2024
- Carpentier A et al. Repeated blood-brain barrier opening with a nine-emitter implantable ultrasound device in combination with carboplatin in recurrent glioblastoma: a phase I/II clinical trial. Nat Commun. 2024 Feb 23;15(1):1650.
2023
- Di Stefano AL et al. In Vivo 2-Hydroxyglutarate Monitoring With Edited MR Spectroscopy for the Follow-up of IDH-Mutant Diffuse Gliomas: The IDASPE Prospective Study. Neurology. 2023 Jan 3;100(1):e94-e106. doi: 10.1212/
- Salam R et al. Cellular senescence in malignant cells promotes tumor progression in mouse and patient Glioblastoma. Nat Commun. 2023 Jan 27;14(1):441. doi: 10.1038/s41467-023-36124-9.
- Hernández-Verdin I et al. Molecular and clinical diversity in primary central nervous system lymphoma. Ann Oncol. 2023 Feb;34(2):186-199.
- Lerond J, Mathon B, et al., Navarro V, Bielle F. Hippocampal and neocortical BRAF mutant non-expansive lesions in focal epilepsies. Neuropathol Appl Neurobiol. 2023 Oct;49(5):e12937.
2022
- Verreault M et al. Identification of growth hormone receptor as a relevant target for precision medicine in low-EGFR expressing glioblastoma. Clin Transl Med. 2022 Jul;12(7):e939.
2020
- Touat M et al. Mechanisms and therapeutic implications of hypermutation in gliomas. Nature. 2020 Apr;580(7804):517-523
2018
- Rosenberg S et al. A recurrent point mutation in PRKCA is a hallmark of chordoid gliomas. Nat Commun. 2018 Jun 18;9(1):2371
- Labreche K et al. Diffuse gliomas classified by 1p/19q co-deletion, TERT promoter and IDH mutation status are associated with specific genetic risk loci. Acta Neuropathol. 2018 May;135(5):743-755.
Membres de l'équipe

Porteur de projet, MD, PhD, MCU-PH, Responsable d'équipe, PI, Sorbonne Université, AP-HP

Porteur de projet, MD, PhD, MCU-PH, Responsable d'équipe, PI, Sorbonne Université, AP-HP

Clinicien, MD, PhD, PH, PI, AP-HP

Chargée de recherche (CRCN), PI, INSERM

Clinicien, MD, PhD, PU-PH, PI, Sorbonne Université, AP-HP

Porteur de projet, MD, PhD, MCU-PH, PI, Sorbonne Université, AP-HP

Porteur de projet, PhD, CRCN, PI, INSERM

Directeur de Recherche, PI, INSERM

Clinicien, MD, PhD (MCU-PH), PI, Sorbonne Université, AP-HP

MD, PhD, Pr (PU-PH), PI, Sorbonne Université, AP-HP