Une étude publiée dans le journal Neurology, conduite par Dario Saracino, Isabelle Le Ber (AP-HP) et leurs collaborateurs, met en évidence l’importance de tester les mutations d’un gène particulier, le gène de la progranuline (GRN), afin de distinguer les aphasies primaires progressives associées à la maladie d’Alzheimer de celles issues d’une dégénérescence fronto-temporale.
Les dégénérescences fronto-temporales (DFT) sont des pathologies particulièrement hétérogènes dont le diagnostic est difficile. Elles prennent des formes différentes qui semblent parfois très éloignées mais qui peuvent appartenir aux mêmes causes génétiques, comme les mutations du gène de la progranuline (GRN). Ces dernières se manifestent habituellement par une variante comportementale de DFT, se caractérisant par des troubles du comportement et des conduites sociales.
« Identifier les mutations génétiques associées aux DFT est capital. Ces maladies n’ont aujourd’hui pas de traitement efficace. L’étude des formes génétiques majeures de ces maladies ouvre la voie à une meilleure compréhension des processus pathologiques sous-jacents et à la possibilité d’intervenir sur ceux-ci par des thérapies innovantes lorsqu’elles seront disponibles. » explique Dario Saracino, neurologue et premier auteur de l’étude.
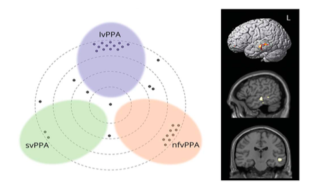
Plus rarement, les DFT peuvent s’exprimer comme des aphasies primaires progressives (APP), avec une atteinte progressive du langage. Les APP se distinguent en trois variantes :
- Non fluente, avec des difficultés à produire ou comprendre des phrases complexes sur le plan syntactique, ainsi que des troubles de l’articulation du langage ;
- Sémantique, avec une perte de la signification des mots ;
- Logopénique, où l’élément principal est le manque du mot.
Les variantes non-fluentes et sémantiques sont clairement associées aux dégénérescences fronto-temporales, ce qui est confirmé par les analyses neuropathologiques dans le cerveau des patients.
Au contraire, la forme logopénique est dans 75 à 85% des cas associée à des lésions de la maladie Alzheimer, avec la présence de plaques amyloïdes et de dégénérescence neurofibrillaire, comme le montrent les études neuropathologiques, ou reposant sur l’analyse des biomarqueurs dans le LCR ou l’imagerie TEP amyloide (PiB). Pourtant, il a récemment été montré que 15 à 20% des patients présentant une aphasie primaire progressive logopénique n’ont pas de lésions typiques de maladie d’Alzheimer (formes dites « amyloïde-négatives »). La ou les causes de ces formes amyloïde-négatives demeurent inconnues.
L’étude conduite par Dario Saracino, Isabelle Le Ber (AP-HP) et leurs collaborateurs, est issue d’un travail multicentrique prospectif qui a débuté il y a plus de 20 ans, réunissant les principaux centres experts des DFT en France, collaborant dans le cadre du Réseau national de recherche sur les DFT. Près de 2 000 patients ont été recensés et un grand nombre de données cliniques, génétiques et d’imagerie ont été collectées par ce réseau. Cette cohorte importante a permis d’étudier une série conséquente de patients atteints d’une APP et porteurs de mutation du gène GRN, pour tirer de plus larges conclusions sur cette forme rare de DFT.
« Aujourd’hui, la recherche sur ces formes de DFT n’a produit que des rapports de cas uniques ou de petite cohorte, qui ne fournissaient pas d’informations cliniquement utilisables, c’est-à-dire les caractéristiques qui face à un patient présentant une aphasie primaire progressive, amenaient à tester des gènes, comme par exemple le gène GRN. »
Les chercheurs ont montré que la forme la plus fréquente chez ces patients avec APP liée à une mutation du gène GRN était la forme logopénique. « Les profils d’imagerie des patients atteints d’une APP logopénique associée à une maladie d’Alzheimer ou à une mutation GRN sont comparables. Cela souligne l’importance de caractériser le profil linguistique de ces patients pour cibler cette forme génétique, une fois la maladie d’Alzheimer écartée. » précise le clinicien-chercheur. L’étude a également permis d’éclaircir les caractéristiques-clés des autres variantes d’APP associées aux mutations de GRN, en particulier les formes non fluentes et mixtes.
Ces découvertes élargissent le spectre clinique associé aux mutations de GRN. Elles permettent de proposer une analyse diagnostique aux patients avec APP logopénique non-amyloïde, et un conseil génétique aux familles de ces patients, ainsi que de les orienter vers des protocoles observationnels et thérapeutiques. Compte tenu des traitements imminents et à venir, il est plus important que jamais de distinguer les APP dues à une mutation du gène GRN de celles liées à la maladie d’Alzheimer.
Sources
https://pubmed.ncbi.nlm.nih.gov/33980708/
Saracino D, Ferrieux S, Noguès-Lassiaille M, Houot M, Funkiewiez A, Sellami L, Deramecourt V, Pasquier F, Couratier P, Pariente J, Géraudie A, Epelbaum S, Wallon D, Hannequin D, Martinaud O, Clot F, Camuzat A, Bottani S, Rinaldi D, Auriacombe S, Sarazin M, Didic M, Boutoleau-Bretonnière C, Thauvin-Robinet C, Lagarde J, Roué-Jagot C, Sellal F, Gabelle A, Etcharry-Bouyx F, Morin A, Coppola C, Levy R, Dubois B, Brice A, Colliot O, Gorno-Tempini ML, Teichmann M, Migliaccio R, Le Ber I; French Research Network on FTD/FTD-ALS.Neurology. 2021 Jul 6;97(1):e88-e102.